Vacuna que se basa en el dominio de la unión del receptor (RBD) de la proteína de la espiga del virus SARS-CoV-2, su segmento más protuberante. Tiene la finalidad de introducir anticuerpos que interfieran con la entrada del agente patógeno a las células: mecanismo que es fundamental en todas las formulaciones de su tipo existentes para generar protección. Esta formulación está adyuvada en hidróxido de aluminio.
La selección de la levadura Pichia pastoris como sistema de expresión se debe a la experiencia del CIGB en el uso de la plataforma tecnológica, más barata en relación con otras y, por tanto, con posibilidad de ventaja en cuanto a gastos de la producción.
Al ser el RBD una glicoproteína asociada covalentemente, los sacáridos de Pichia pastoris le aportan un efecto inmunopotenciador que favorece la inmunogenicidad. De hecho, Abdala no necesita proteína portadora para alcanzar elevados niveles de este indicador, evaluado en las fases I-II del estudio clínico.
Se diseñó por medio de ingeniería de proteínas, con el empleo de métodos computacionales de bioinformática estructural, encaminados a incrementar su similitud con el virus SARS-CoV-2.
La proteína creada destaca por su versatilidad, en tanto puede utilizarse como inmunógeno solo, y en forma de nanopartícula híbrida.
Estudio clínico Fase III de Abdala
92.28%
Eficacia frente a la enfermedad sintomática
100%
Eficacia en la prevención de la enfermedad sistémica severa y del fallecimiento de vacunados
90%
Efectividad en pacientes graves
Suspensión para inyección
Inyección intramuscular
- Estuche por 6 estuches individuales conteniendo 1 bulbo con 10 dosis de 0.5 mL cada uno
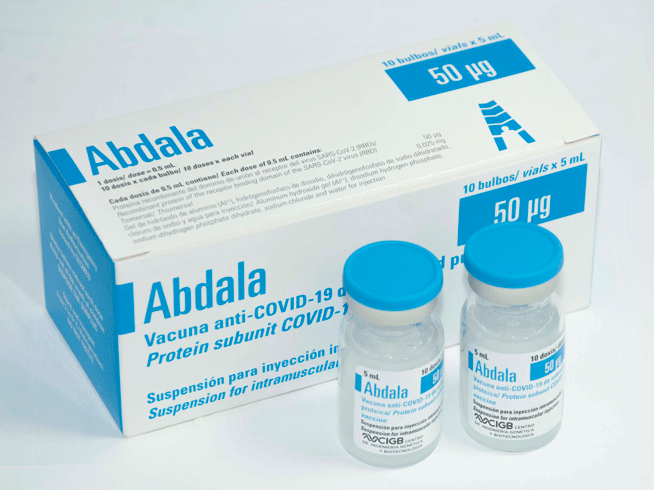
- Estuches por 10 bulbos conteniendo 10 dosis de 0.5 mL cada uno
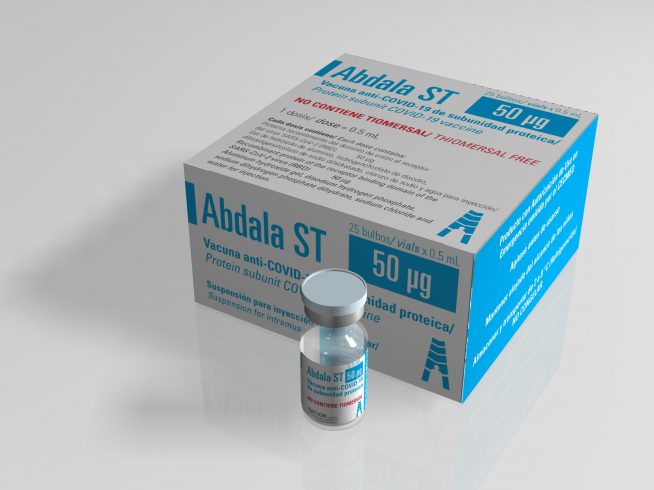
- Estuches por 25 bulbos conteniendo 1 dosis de 0.5 mL cada uno
Cada 0.5 mL contiene:
- Proteína recombinante del dominio de unión al receptor del virus SARS-CoV-2 (RBD) 0.05 mg
- Tiomersal 0.025 mg
- Gel de hidróxido de aluminio (Al³+)
- Hidrogenofosfato de disodio
- Dihidrogenofosfato de sodio dihidratado
- Cloruro de sodio
- Agua para inyección, c.s.
La vacuna debe almacenarse entre 2 y 8 ºC. NO CONGELAR; DESECHAR LA VACUNA SI SE CONGELA.
- Se extremarán las medidas higiénico-sanitarias y de bioseguridad durante la inoculación del producto y para la eliminación de los materiales utilizados.
- Para cada inyección debe utilizarse una jeringuilla y una aguja estériles.
- Al completar la aplicación intramuscular, desechar el bulbo, la aguja y la jeringa.
- Una vez administrado el producto, NO retapar nuevamente la aguja utilizada. Se debe desechar en depósitos designados para ello.
- Los bulbos multidosis que no se hayan utilizado completamente en una sesión de inmunización, NO se pueden conservar para utilizarse en sesiones subsiguientes y deben ser desechados al final de la sesión de inmunización.
Posología
Tres dosis separadas por intervalos de 14 días (esquema 0-14-28 días).
Modo de administración
- El producto se administrará por la vía intramuscular: 0.5 mL en la región deltoidea del brazo (parte superior externa); preferentemente en el brazo no dominante.
- Las inmunizaciones se realizarán por personal de enfermería capacitado y en vacunatorios certificados para esta actividad.
- Para la administración del producto se utilizarán jeringuillas de 1 mL de volumen, rotuladas con 10 divisiones, y con agujas 23 G o 22 G x 25 mm.
- AGITAR SUAVEMENTE ANTES DE EXTRAER CADA DOSIS.